University Göttingenらのグループは、ミンクにSARS-CoV-2が感染し、ミンクで発生した変異ウイルスがヒトに感染してくる可能性を議論しています。
https://pubmed.ncbi.nlm.nih.gov/33857422/
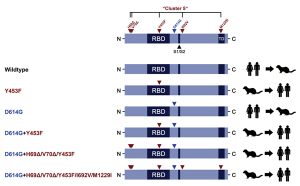
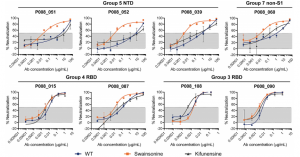
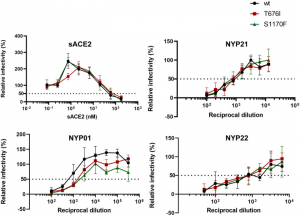
SARS-CoV-2が家畜として養われているミンクにヒトから感染したことが欧州および米国で見つかりました。ヒトにおける代表的な変異であるD614Gもミンクで見つかり、ミンク特有な変異Y453F(変異 D614G+Y453F)、更にはH69Δ、H70Δも見つかりました(変異 D614G+H69Δ/H70Δ/Y453F)。Y453F変異はRBDの中にあり、ヒトの血清サンプル評価では、IC50が1.62倍増加し、感染阻害が低下していました。また、カクテル抗体治療薬であるREGN-COV2(casirivimab/REGN10933)のREGN10933でも感染阻害が低下していました。
SARS-CoV-2が野生動物中で更なる変異を生む可能性が危惧されます。