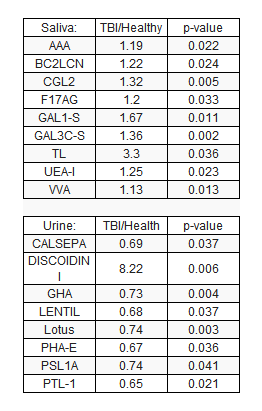
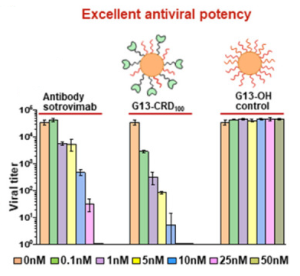
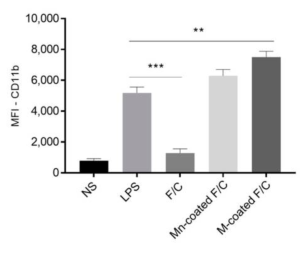
比較糖鎖プロファイリング解析において、レクチンマイクロアレイは、絶大なる力を発揮します。更には、レクチンマイクロアレイの解析にエバネッセント波蛍光励起法を使用することにより、レクチンと糖鎖との弱い相互作用を非破壊でモニタリングすることが可能であり、世界最高レベルの比較糖鎖プロファイリングを行うことが可能です。
本技術の詳細については、下記をご参照ください。
Products & Services
さて、今日現在、世界には製造元が明らかでないレクチンマイクロアレイも幾つか存在しますが、商業ベースで製造販売されているものも数品種存在しています(PSS、RayBiotechなど)。
そこで、ここ数年のレクチンマイクロアレイが使用されている論文を参照しながら、その品質を公開されている画像から比較検討してみたいと思います。
結論から言えば、LecChipに勝る品質を持ったレクチンマイクロアレイは存在しないと言って良いでしょう。
LecChip made by GlycoTechnica(現在は、PSSにて製造販売されている)

Lectin microarray made by RayBiotech (https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10348014/)
スポットサイズはバラバラ、
非常に小さいスポットも存在、
中抜けしてリング状になっているスポットも存在

Lectin microarray, unknown manufacturer (https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6636412/)
スポット内に斑が存在する、恐らくピンタイプのスポッターで製造していると推測される
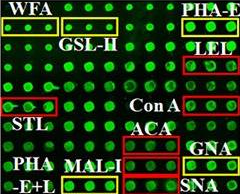
Lectin microarray, unknown manufacturer (https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8798758/)
スポットの中抜けが強烈
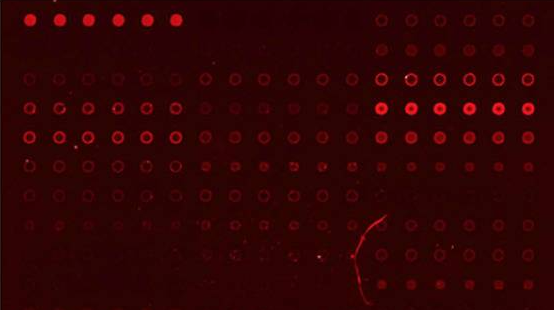
Lectin microarray, unknown manufacturer (https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9772556/)
スポットの形状異常、
スポット内の斑が劣悪、
スポット抜けも見受けられる
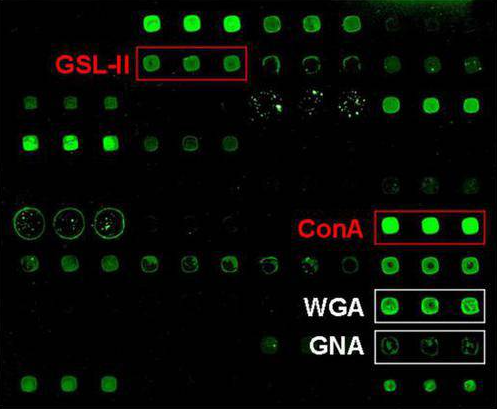
Lectin microarray, unknown manufacturer (https://www.frontiersin.org/articles/10.3389/fchem.2021.637730/full)
スポットの中抜けを除けば比較的良好だが、
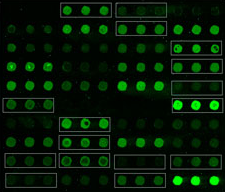
Lectin microarray, unknown manufacturer (https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7840895/)
スポット形状がバラバラ、
スポット内の斑も劣悪