Faculty of Science and Engineering, Swansea University, Singleton Park, Swansea SA2 8PP, Wales, UKらのグループは、昆虫病原性糸状菌によって産生される天然の抗菌性揮発性有機化合物は、植物の天然バイオ農薬として使用できる可能性があると報告しています。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9025432/
昆虫病原性真菌は植物と共生関係を築き、植物の成長と生産性を向上させます。 Metarhizium brunneumやBeauveria bassianaなどの昆虫病性真菌種で処理された植物は、通常、未処理の植物よりも根系が大きく広がり、バイオマスも増え、収穫量が多くなります。
本研究では、これらの昆虫病原性真菌によって産生される真菌抗菌性揮発性有機化合物の抗菌特性を、次の土壌微生物を用いて評価しています。
グラム陰性バクテリア (Escherichia coli, Pantoea agglomerans, Pseudomonas aeruginosa)、
グラム陽性バクテリア (Micrococcus luteus, Staphylococcus aureus, Bacillus subtilis, B. megaterium, B. thuringiensis)、
酵母 (Candida albicans, Candida glabrata)、そして
植物病原性真菌 (Pythium ultimum, Botrytis cinerea, Fusarium graminearum)。
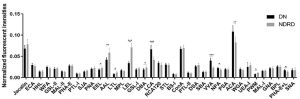
最も強力な抗菌剤はisovaleric acidと1-octen-3-olであり、バクテリア、酵母、糸状菌、卵菌らの成長を阻害したり殺傷しました。また、isoamyl formate、3-octenone、cedrene、farneseneらも強力ではありますが、土壌微生物に対する特異性がより制限されていました。一部の微生物は、他の微生物よりも明らかにM. brunneumが産生する抗菌性揮発性有機化合物に敏感でした。感度の順に並べると、F. graminearumは、他のどの試験微生物よりもはるかに多くの化合物によって阻害され、次にB. cinerea、次にP.ultimumとなりました。試験微生物のうち、B. megateriumが最も感受性が高く、B. thuringiensisがそれに続く結果となりました。
本研究で特定された天然の抗菌性揮発性有機化合物は、植物の天然バイオ農薬として使用できる可能性があります。