3月中旬、ムスカリが咲き始めました。早春の青紫がとても奇麗です。近寄ってみるとブーンという羽音と共に何匹ものミツバチがムスカリに群れていました。のどかな早春の風景です。
キラーアプリの開発と標準化が糖鎖ビジネスを成功させるには必要だ
iGCOREが主催する第9回糖鎖技術研究セミナー(2026年1月9日開催)のお題は「糖鎖ビジネスを成功させるには何が必要なのか~糖鎖プローブレクチンの活用例と標準化~」でした。このセミナーに嬉しいかな本ブログ管理人(山田雅雄)と㈱QuastellaのCSOである加藤竜司様がプレゼンターとして招待を受けました。自分がこの場でお話させて頂いた内容を忘備録を兼ねて本ブログ記事として書き下ろしてみたいと思います。
合同会社エムックのご紹介
世界でいち早くレクチンマイクロアレイの商業化を進めた事業体のひとつがモリテックスのグライコミクス研究所であり、2007年に糖鎖プロファイリング・システム”GlycoStation”を上市しています。当時のグライコミクス研究所の所長は本ブログ管理人でした。この技術は、モリテックス→GPバイオサイエンス→グライコテクニカと変遷をうけつつも、Mx(エムック)に受け継がれて現在に至って至っています。
レクチンアレイの登場とプレーヤー
レクチンアレイの商業化は、日本のMoritex(GlycoStation)とイスラエルのProcognia(GlycoScope)が先駆けでした。モリテックスからスピンアウトしたGP Biosciences(2009年2月27日設立登記)は、遡ること2008年11月、ロンドンで開催されたグライコミクス研究所の代表者とプロコグニアの代表者が介しての特許紛争に関する合意によって花開いたものです。しかし、皮肉なことに先行する二社は、2013年から2014年にかけて相次いで倒産してしまいます。この出来事がきっかけとなり、Procognia特許がOpen化されたことでレクチンアレイに対する参入障壁が大幅に低下し、ビッグバンが起こります。因みにGlycoStationの基本は、産総研が持つエバネッセント波蛍光励起法を用いたレクチンアレイの非破壊読み出しに主眼点がありました。ともあれ、ビッグバン後に新規参入してきた事業体はこつぶであり、巨大資本がなだれ込んで来たわけではありません。まだまだマーケットが未熟であったことが原因です。

世界情勢の変化
事業戦略を立てる上において、世界の潮流をきちんと認識しておくことは非常に大切です。昨今は、グローバリズムから反グローバリズムの方向に大きく舵が切られており、これは歴史的にも特質すべき世界情勢の変化です。グローバリズム下においては、巨大資本へ権力が集中し、それによって格差の拡大が益々加速し、更には文化の壁を越えて世界の均質化が進みます。一党独裁のC国がこのグローバリズムと相性が良いというのは皮肉的です。
反グローバリズムの動きは、各国の動きをみると明確です。例えば、米国では第二次トランプ政権が発足し、トランプ関税が世界を席巻しています。日本では参政党らの保守勢力が勢いづき、高市政権が誕生しています。フランスでは国民戦線が躍進、ドイツではAfDが躍進、そしてイタリアではメローニ政権が誕生しています。この結果として、自国ファーストを合言葉に世界的な製造業の国内回帰とC国とのデカップリングを伴うサプライチェーンの再構築が進行しています。日本では、半導体の復権を目指して、政府肝いりのRapidusの立ち上げやTSMCの誘致が行われています。更には、国力の向上に大切な先端技術分野(AI、量子技術、核融合など)への研究開発投資が加速しています。
日本の産学連携はまだ中途半端
国力の増強という観点からは、現在の日本の産学連携はまだまだ中途半端であり、最終的な出口で勝負ができるような運営形態に変えていく必要があります。
シーズの開発に必要な基礎研究は、それほどリソースが無くても可能です。日本はシーズ開発では先行するものの、開発した技術の多くが大規模化の段階で諸外国(中国、台湾、韓国ら)に敗北しているという事実を強く問題視する必要があります。液晶パネル、半導体、造船、ソーラーパネルなど・・枚挙にいとまがありません。儲けるべきところで失敗しているわけですからGDPが増えるはずもありません。失われた30年間、負け犬癖がついてしまった日本ですが、「MAKE JAPAN GREAT AGAIN」を実現するためには意識改革が必要です。
国力を高めるための政府の戦略的な大規模支援が必要です。製造業の国内回帰と強化が反グローバリズム時代の基本戦略です。支援した先が儲かれば、政府の税収が増え、その資金は新たな研究開発支援に回ることで好循環が生まれます。大局的な観点からリソースの再配分を考えることが大切です。基礎研究を支援しベンチャー設立を支援したらそれで国の役割は終わりだ、「汚い金儲けの仕事は民間でやれ!」こういう意識が蔓延してないでしょうか?再度になりますが、儲けるべきところで儲けられなければジリ貧になる一方です。GDPが増えるわけもありません。産業界においても、大規模な企業連合体(株式持ち合いによる護送船団)を作り世界の巨大資本と伍して戦う体力と気概を持たねばなりません。国力を高めねば、基礎研究費も出なくなり、結果としてノーベル賞の受賞も減少していくでしょう。
産業を大きくするには標準化が必要
技術の標準化を進めると、参入障壁が下がり、競争によってコストも下がり、ユーザーが爆発的に増えます。PCのWindowsの世界観がまさにそれです。標準化によって、得意な分野にリソースを集中できることから分業化も進行します。
糖鎖関連では、例えば、ヒトに発現する網羅的な糖鎖の標準ライブラリー、リコンビナント化されたレクチンの標準ライブラリー、糖鎖構造解析ツール、更には分析・解析プロトコルなどの標準化が必要です。
キラーアプリの開発こそ要
シーズだけを開発してもダメ、ベンチャーを作ったらお終いではダメ、巨大な潜在マーケットを持つであろうキラーアプリがないと、人も金も集まりませんし、そこまでは最低限支援することが必要です。
糖鎖関連では、誰が何の為に糖鎖ライブラリーを使用するの?誰がどういう目的でレクチン・ライブラリーを使用するの?誰が高価な糖鎖解析ツールを使用するの?そういった事業化の目標設定に際して「儲かるキラーアプリ」を明確にイメージしなければなりません。
糖鎖は表現型であり、「細胞の顔」とも呼ばれる生体分子ですから、診断薬は糖鎖に対しては良いターゲットに成り得ます。例えば、AFP-L3やM2BPGiなどの実例を挙げることができます。ブログ管理人自身も、潰瘍性大腸炎、IgA腎症、そしてうつ病らの診断薬開発に取り組んだ経験があります。しかし、最終的に糖鎖関連事業が勝者になるためには、糖鎖創薬に繋がるキラーアプリを見つけなければならないでしょう。
潜在的キラーアプリの実例
本ブログ管理人が事業視野に入れる領域から、潜在的なキラーアプリの実例をご紹介したいと思います。これは、2013年から10年以上に渡って行ってきたFDAとの共同研究開発の成果物です。具体的には「治療用抗体の簡易ハイスループット糖鎖プロファイリングをカスタム・レクチンアレイで行う」という内容です。
FDAはすでに157種類の抗体医薬品を認可していますが、それらを網羅的に概観し、抗体医薬品の発現系やIgGのサブタイプについて報告しています。発現系としては、76%がCHOであり、78%がIgG Type 1であることが分かります。

治療用抗体(mAb)によくみられる9つの糖鎖エピトープ
FDAによるmAbに一般的に存在する9つの糖鎖エピトープの発見と同定は、治療用mAbの糖鎖修飾に対する貴重な洞察と貢献を与えるものです。9つの糖鎖エピトープとは、core fucose, terminal N-acetylglucosamine, terminal β-galactose, high mannose, terminal α2,3-linked N-acetylneuraminic acid, terminal α2,6-linked N-glycolylneuraminic acid, bisecting N-acetylglucosamine, terminal α-galactose, triantennary structureであります。
この情報は、mAb製造中の糖鎖修飾パターンを評価および監視し、製品品質の一貫性を確保し、薬物動態や免疫原性の変化につながる可能性のある望ましくない糖鎖プロファイルのリスクを軽減するために不可欠なものであります。
治療用mAbの迅速な糖鎖プロファイリングのためのカスタム・レクチンアレイ
糖鎖修飾は治療用mAbの品質と有効性を決定する上で重要です。FDAは、前述した9つの糖鎖エピトープを正しく評価するために、各糖鎖エピトープに対応する9つの異なるレクチンを特徴とするカスタム設計されたレクチンアレイを導入しました。そのレクチンは、rPhoSL, rOTH3, RCA120, rMan2, MAL_I, rPSL1a, PHAE, rMOA, PHALの9種類であります。2種類ほど一般名ではないレクチンがありますが、諸事情がありましてご容赦お願い致します。これら一連の作業は、GlycoTechnicaとの共同作業として実施され、当時GlycoTechnicaが使用していた83種類のレクチンの中からFDAが厳選したものです。
IgG1-mAb-LecChipと命名されたこのレクチンアレイは、糖タンパク質サンプルから糖鎖を切り出すことなくそのまま利用することが出来、迅速な糖鎖プロファイリングのためのハイスループットプラットフォームを提供し、糖鎖修飾パターンの比較分析を可能にします。FDAは、このレクチンアレイが、様々な製造バッチ間、あるいはバイオシミラーと先発医薬品間の糖鎖修飾の違いを評価する上で極めて実用的であるとその使用を推薦しています。

mAbs間の糖鎖修飾パターンの違いをいとも簡単に捕まえることができる
NISTの標準抗体をコントロールとして、4種類の治療用mAb(Filgrastim, Atezolizumab, Trastuzumab, Cetuximab)の比較糖鎖プロファイリングの例が示されています。左側は低感度スキャンであり、右側は小さい信号のレクチンが良く見えるように高感度でスキャンしたものを示しています。MS解析とは異なり、9種類の糖鎖エピトープの発現状態の違いが手に取るように分かります。下段は、左からcore fucoseの有無をrPhoSLで見た場合、tri/tetra-antennaryの有無をPHALで見た場合、α2-3Siaとα2-6Siaの発現状態の違いをMAL_IとrPSL1aで見た場合を示しています。ものの見事に判別できていることが分かります。

以下に示す例は、Infliximabの先行品とその3種類のバイオシミラーとの糖鎖プロファイリングの比較です。上記と同様に、左側は低感度スキャン、右側は高感度スキャンを示しています。Agalacto, High mannose, α2-6Siaらに大きな違いがあることが一目瞭然です。このようにして、FDAは、IgG1-mAb-LecChipが、様々な製造バッチ間、あるいはバイオシミラーと先発医薬品間の糖鎖修飾の違いを評価する上で極めて実用的であるとその使用を推薦したのです。

もちろん、治療用mAbに発現する糖鎖構造については、MS解析による構造同定のデータを示すことが許認可には必須とされており、レクチンアレイのみのデータを持って許認可が今日現在出るわけではありません。しかしながら、MS解析による糖鎖構造同定とレクチンアレイによる比較糖鎖プロファイリングは補完的な情報を与えるものであり、お互いがお互いの存在を否定しあうものではないことをここで明言しておきたいと思います。
世界の医薬品全体のマーケットサイズは2024年に約262兆円に達しています。その中でもバイオ医薬品の成長は顕著であり、同年にはそのマーケットサイズは38兆円に達し、今後も10%を超える成長率が見込まれています。更に、世界売上高の上位100位の医薬品に絞ると、バイオ医薬品の占める割合は2019年には5割以上を占めるまでになっています。現存するマーケットの大きさとその成長性を鑑みれば、IgG1-mAb-LecChipというアプリケーションは、正に潜在的なキラーアプリに成り得る可能性を持っているということができるでしょう。
糖鎖創薬に対する新たな視点
治療用mAbの成功により、タンパク質と糖鎖を両睨みすることでターゲティング性能を改善するという視点から糖鎖を抗原とする抗糖鎖抗体の開発が良く議論されています。しかしながら、この観点での糖鎖創薬はいまだに成功例がほとんどありません。なぜ抗糖鎖抗体が作り難いのか?というお話にはここでは踏み込みませんが、その代わりとなる糖鎖創薬の視点に話を変えてみたいと思います。
糖鎖は、ご存じのようにありとあらゆるところに存在しているがために、すべての生命現象に関与する生体分子として糖鎖創薬の目標が大風呂敷になりがちなのではないでしょうか?ブログ管理人はすべての糖鎖が絡んだ事象を網羅できているわけではないのですが、思うに、糖鎖が絡んだ超厳格なプロセスはかなり例外的なように思います。その例がここに示すカルネキシン/カルレティキュリン・サイクルによるタンパク質のフォールディング品質管理です。G3M9型糖鎖(G:グルコース, M:マンノース)がリボソームから翻訳された新生ペプチドに付加します。GlucosidaseⅠ, ⅡによってG1M9型糖鎖に刈り込まれ、それがフォールディングを助けるタンパク質であるCNX/CRTなどのシャペロン分子により特異的に認識され、フォールディングがおこなわれます。その後GlucosidaseⅡによってM9型糖鎖に刈り込まれ、この時点で正しくフォールディングしていれば、次の段階であるゴルジ体へ輸送されていきます。正しい三次元構造をとれていない場合、UGGTというフォールディングセンサー酵素に捕らえられ、グルコースが一つ再付加されG1M9糖鎖に戻り、上記のループを繰り返します。このプロセスでは、ヘテロな糖鎖発現は全く存在せず、Glc=1個の付加がタンパク質の命運を分けています。あり得ないほど超厳格なプロセスです。糖鎖の存在と役割がこのように超厳格である場合には、それをピンポイント的にターゲティングすることでその下流にあるシグナル伝達経路を遮断することが可能になり、創薬としては創薬ターゲットがとても絞りやすくなります。
しかしながら、糖鎖は、一般的にはヘテロな集団として生化学反応に関与していますので、その視点から糖鎖創薬の方法論を考え直してみるべきではないでしょうか?
ヘテロな糖鎖とプロファイリング技術の重要性
糖鎖が遺伝子によって直接コーディングされていないこともあり、糖鎖の発現は自由度が高くヘテロな分子集団を形成します。皆様には釈迦に説法的なお話ですが、下記にはIgGに発現する糖鎖をMSにて詳細解析した例が載せられています。MS解析では非常に数多くのピークが観測され、二分岐N‐型糖鎖が基本であるものの、数多くの派生構造が雑多に発現しています。しかし、ADCCやCDCと言った機能的な観点からは詳細構造情報よりもエピトープの比較プロファイリングでその増減が分かれば実際には十分であります。この種の目的には、糖鎖プロファイルの変化を簡単に解析できるレクチンアレイを用いた比較糖鎖プロファイリングが極めて有効であります。

承認されている治療用mAbに対する糖鎖の記述は貧弱
国立医薬品食品衛生研究所)生物薬品部のホームページには、認可されたバイオ医薬品の一覧が記載されています。各バイオ医薬品の審査報告書も公開されています。治療用mAbの幾つかを覗いてみたのですが、糖鎖に関する記述が貧弱なのに正直驚きました。記載されているのは主だった糖鎖構造とそのタンパク質への結合位置に対する情報のみです。糖鎖はヘテロな集団なのに、ヘテロな存在割合やそれが薬効や副作用にどのように関係しているのか?何も記載がありません(報告書は長いので斜め読みしている関係で読み飛ばしている可能性もありますが、目に止まらないくらい糖鎖に対する記述が少ないということです。これは糖鎖関連技術を開発している我々にとっては由々しき事態です。)ブログ管理人にとっても、そもそもヘテロな糖鎖集団と単一糖鎖構造の間で一体どの程度の差異が薬効に現れるのかすら明確でありません。
しかしながら、協和発酵キリンのポテリジェント技術が有名であるように、糖鎖の存在が薬効に影響を与えることは事実です。ブログ管理人が過去に、ノバルティスとスタンフォード大学との共同研究を行った結果を一つお見せ致します。以下に示す例は、当論文からの抜粋ですが、IL-23RをCHO細胞とHEK細胞で発現させた場合の違いを見せています。尚、この例はマウスでの実験です。in vitroでの実験では、両者に全くの違いは見られなかったのですが、in vivoでは、面白いことに血中濃度に極めて大きな濃度差が見られています。つまり同じ薬を作ったつもりでも、糖鎖が違うだけでこれだけ血中濃度(効果)が変わるということを如実に示しています。

名わき役にこだわり抜くと発見があるかも
先ほどご紹介した国立医薬品食品衛生研究所のホームページに記載されている認可済みのバイオ医薬品(治療用mAbのみでなく、酵素やサイトカインやホルモンなども幅広く)ですが、このような情勢を鑑みれば、その医薬品に発現している糖鎖構造が最適化されたものなのか?それとも単に発現した結果なのか?については、知る由もありません。しかし、実際には、発現している糖鎖が薬効に関係することは事実として例が幾つもある訳ですから、既存の医薬品に対しても糖鎖構造を改変してあげることで容易に「バイオベター」が得られる可能性があります。既に認可されている医薬品ですから、糖鎖構造の改変だけならレギュラトリーの閾値は下がるはずですし、すでにマーケットが存在している訳ですから、その開発リスクも少なくて済みます。実際にこれをやるかどうか?は、認可を取った製薬メーカーの考え方次第かも知れません。今更めんどくさいよ、やるだけの効果ほんとに出るのかな、いろいろな意見があることでしょう。どう考えるかはあなた次第です。
糖鎖の主たる機能は何なのか?
糖鎖がありとあらゆるところに存在し、ありとあらゆる分子間信号伝達に程度の差はあれ関わることから、糖鎖の機能について語る場合に、あれもこれもと話が大風呂敷になりがちです。その結果として創薬ターゲットの絞り込みが困難になります。糖鎖が持つ本当に重要な機能は、自分が考えるに、下記の二種になるのではないでしょうか?
自然免疫:怪しい糖鎖構造を持つ外来異物を総当り的に攻撃して排除する(自己と非自己の認識)
ブロッキング:糖鎖がリガンドと受容体の相互作用をブロッキングすることで下流のシグナリングを制御する
糖転移酵素の局所的な制御技術こそ最終的な目標か
糖鎖創薬に対する考え方なのですが、ブログ管理人は、糖鎖が持つ最大の機能である自己と非自己との判別を利用した自然免疫という原点に戻ってみることが面白いと思います。
Siglec/シアル酸の免疫チェックポイントに対する創薬はがん治療という観点ですでに研究開発が本格化しています。ここで更に踏み込んで、がん細胞に発現する糖鎖構造を大幅に制御してみてはどうでしょうか?
例えば、がん細胞に特異的にターゲティングさせた糖転移酵素の発現阻害で癌細胞の糖鎖構造をハイマンノースに変えてしまうのです。そうすると、自然免疫が活性化し、マクロファージやNK細胞ががん細胞を食い尽くしてしまうのではないでしょうか?この種の試みは、ブログ管理人が知る限りにおいて全世界においても全く手つかずであるように思います。がんが撲滅できれば、これ以上にインパクトのある創薬はありません。弊社ではリソース的に取り組むことが難しく、どなたかご興味があれば、是非やってみて頂けないか?と勝手に考えております。あるいは、iGCOREを起点にして共同開発チームを作れないか?などと妄想しています。実際に行う場合には、上記した以外の派生方法もあるかもしれませんが、ともあれがん細胞へのターゲティング方法が一番の課題かも知れません。
潰瘍性大腸炎の患者ではシアル酸アセチル化が減少している
Center for Clinical Mass Spectrometry, College of Pharmaceutical Sciences, Soochow University, Suzhou, Jiangsu, Chinaらのグループは、SIAEを介したシアル酸アセチル化の減少が潰瘍性大腸炎の特徴となっていると報告しています。
https://pmc.ncbi.nlm.nih.gov/articles/PMC12011031/
本研究では、質量分析法により、潰瘍性大腸炎患者のタンパク質および糖タンパク質の変化が健常者と比較されています。
潰瘍性大腸炎患者の組織ではシアル酸とそのアセチル化が減少しているのに対し、健常者ではシアリル化とO-アセチル化がより多くみられることが明らかになりました。
シアル酸は、特にアセチル化された状態では、免疫細胞間の相互作用を調節するメカニズムを通じて炎症を防ぎ、腸壁を有害な細菌から保護することで、腸内での過剰な免疫反応に対するバリアとして機能し、大腸において保護的な役割を果たしているとの見解です。
ガレクチンは単なるβ-ガラクシド結合型レクチンではなく多面的な機能を持っている
Axe of Infectious and Immune Diseases, CHU de Quebec-Université Laval Research Centre, Faculty of Medicine, and Research Centre for Infectious Diseases, Laval University, Quebec, Canadaらのグループは、宿主免疫におけるガレクチンの多面的な機能についてレビューしています。
https://www.sciencedirect.com/science/article/pii/S1044532324000642?via%3Dihub#bib63
他のレクチンとは異なり、ガレクチンはシグナルペプチドを欠いているため、糖鎖リガンドが存在しないサイトゾールで可溶性の非糖化タンパク質として合成されます。さらに、ガレクチン-1 やガレクチン-3 などの特定のガレクチンは、特定の条件下で核に移行することがわかっています。これは大きな矛盾です。何故ならば、ガレクチンの主な存在位置はサイトゾールであり、ガレクチンが結合する糖鎖が存在しない環境だからです。
しかし、興味深いことに、ガレクチンは、非古典的でリーダーのない分泌経路を介して細胞外空間に分泌されることもできます。
細胞内外のガレクチンのこの独特な分布は、ガレクチンの機能の多用性を示しており、宿主防御におけるガレクチンの機能がその合成とリガンドへのアクセスの空間的制御の両方によって調節されることを可能にする重層的な調節機構が存在することを示唆しており、ガレクチンの進化的役割は従来の糖鎖認識を超えて拡張されているようです。
非常に興味深いレビューとなっており、ご一読をお勧めします。
ALAレクチンが胆管癌の治療に有効かもしれない
Department of Biochemistry, Faculty of Medicine, Khon Kaen University, Thailandらのグループは、モンキーフルーツの種から抽出された新規レクチンALAについて報告しています。
https://www.nature.com/articles/s41598-024-84444-7
ALAは凝集素活性を示し、T- および Tn-抗原および単糖類 (Gal や GalNAc など) に対して糖鎖結合特異性を示しました。
ALAによって認識される糖鎖がヒト胆管癌 (CCA) 組織で増加していることが確認されました。ALAは、CCA 細胞、KKU-100 および KKU-213B、の細胞生存率をドーズ依存的に大幅に低下させ(最大 30 μg/mL まで)、最高濃度では約 30% の低下が観察されました。また、ALAは、細胞生存率には影響を与えない1 ~ 2 μg/mL の濃度でドーズ依存的に KKU-100 および KKU-213B 細胞の遊走および浸潤能力を大幅に低下させました。
これらの結果は、CCA治療に対するこのレクチンの潜在的な治療効果を示唆しているようです。
海の動植物から発見されたレクチンの糖鎖結合特異性
School of Medicine and Life Sciences, Far Eastern Federal University, Vladivostok, Russiaらのグループは、海の動植物から発見されたレクチンとその脳腫瘍の診断や治療への応用について報告しています。
https://pmc.ncbi.nlm.nih.gov/articles/PMC11679326/
HOL-18:marine sponge Halichondria okadai由来レクチン、複合型N-型糖鎖に結合
OXYL:marine star Anneissia japonica由来レクチン、LacNAc type 2には結合するが、LacNAc type 1には結合しない
AVL:marine sponge Aphrocallistes vastus由来レクチン、シアリルムチンに結合
ESA:seaweed Eucheuma serra由来レクチン、high mannose N-型糖鎖に結合
UPL1:seaweed Ulva pertusa由来レクチン、GlcNAcとhigh-mannose N-型糖鎖に結合
BPL2:seaweed Bryopsis plumosa由来レクチン、trimannosyl coreに結合
KSL:red alga Kappaphycus striatus由来レクチン、high mannose N-型糖鎖に結合
DIFBL:sea bass Dicentrarchus labrax由来レクチン、fucoseに結合
APL:starfish Asterina pectinifera由来レクチン、Tn antigenに結合
CGL:bivalve Crenomytilus grayanus由来レクチン、GalNAc/GalおよびGb3に結合
MytiLec:Mediterranean mussel由来レクチン、Gb3に結合
HCL:marine sponge Haliclona cratera由来レクチン、GalNAc/Galに結合
DTL:ascidian Didemnum ternatanum由来レクチン、GlcNAcに結合
乾癬性関節炎(PsA)と関節リウマチ(RA)を区別できる新規糖鎖マーカー
Division of Laboratory Diagnostics, Department of Laboratory Diagnostics, Faculty of Pharmacy, Wroclaw Medical University, Polandらのグループは、乾癬性関節炎(PsA)と関節リウマチ(RA)を区別するための新規糖鎖マーカー、即ち血清クラステリンの糖鎖修飾変化、について報告しています。
https://www.mdpi.com/1422-0067/25/23/13060
PsA および RA は結合組織自己免疫疾患です。
本研究は、血清クラステリン (CLU) 濃度とその糖鎖修飾パターンがこれらの疾患を区別できるマーカーである可能性があるかどうかについて研究しています。
結果、以下の事柄が判明しました。
RA患者の血清中のCLU濃度は、PsA群と比較して有意に低く、CLU濃度に関しては、検査した群間にその他の有意差はありませんでした。
CLUに発現する糖鎖と SNA (α2-6 Sia 結合レクチン) の相対反応性は、対照群と比較して、RAおよびPsA患者で有意に高く、CLUに発現する糖鎖とMAA (α2-3 Sia 結合レクチン) の相対反応性においては、研究グループ間に有意差はありませんでした。
これらの結果は、CLU濃度とシアル酸修飾(by SNA)によってPsAとRAが区別できることを示しています。
SARS-CoV-2の感染をβ1-4ガラクトシル化N型糖鎖で阻害することが出来る
Laboratory for Functional Glycomics, College of Life Sciences, Northwest University, Xi’an 710069, Chinaらのグループは、SARS-CoV-2の感染をβ1-4ガラクトシル化N型糖鎖で阻害することが出来ると報告しています。
https://www.sciencedirect.com/science/article/pii/S2090123224005666?via%3Dihub
SARS-CoV-2-Spikeタンパク質(S1)には22個の潜在的なN型糖鎖修飾サイトと17個のO型糖鎖修飾サイトがあり、そのうち14個のN型糖鎖修飾サイトは複合型N型糖鎖で装飾されており、ACE2には合計7個のN型糖鎖修飾サイトが存在し、これらの部位のほとんどは複合型N型糖鎖によって占められていることが既に分かっています。
本論文では、ACE2のβ1-4ガラクトシル化N型糖鎖が SARS-CoV-2のS1結合の糖鎖受容体として重要な役割を果たしていることが実証され、多価β1-4ガラクトシル化N型糖鎖を含む単離された糖タンパク質が、S1とACE2間の相互作用を競合的に阻害し、それによって宿主細胞へのSARS-CoV-2の付着と侵入が防御されると述べられています。今更感がある論文かもですが紹介させて頂きました。
Tn-抗原を標的とすることで、乳癌の転移を抑制することが出来る
Department of Gynecology and Obstetrics, Beijing Chao-Yang Hospital, Capital Medical University, Beijing, Chinaらのグループは、Tn-抗原を標的とすることで、乳癌の転移を抑制することが出来る、と報告しています。
https://onlinelibrary.wiley.com/doi/10.1111/jcmm.70279
Tn-抗原は乳癌、特に転移性病変内で高発現しており、Tn-抗原の発現は、リンパ節転移および患者の生存率の低下と正の相関関係がありました。Tn-抗原を発現する乳がん細胞においては、上皮間葉転換およびFAKシグナル伝達経路の顕著な活性化とともに、浸潤性と転移能が向上していました。
Tn-抗原を発現する癌細胞では、標準的な上皮マーカーであるE-カドヘリンとZO-1の大幅な発現低下があり、ZEB-1、ビメンチン、カタツムリ、ナメクジなどの間葉系マーカーの大幅な発現上昇も見られました。
HPAレクチンを用いてTn-抗原陽性癌細胞を標的化することで、浸潤および転移能力が抑制されることが実証されました。HPAレクチンは、Tn-抗原を特異的に認識して結合するのに対し、PNAレクチンは、T-抗原のみを認識して結合することが知られています。PNAで処置した対照群と比較して、HPA処置群のマウスは肺転移の有意な減少を示しました。更に、免疫蛍光分析は、HPA処理が Tn-抗原陽性癌細胞の細胞突起の形成を減少させるのに対し、PNA処置は、阻害効果を示さないことも示されました。分子レベルでは、上皮間葉転換およびFAKシグナル伝達経路は、HPAで処理したTn-抗原陽性癌細胞で一貫して阻害されていることが分かりました。
うつ病の血中糖鎖マーカーが見つかる
山口大学医学部神経精神医学らのグループは、うつ病に対する新しい糖鎖マーカーについて報告しています。
https://www.nature.com/articles/s41598-024-80507-x
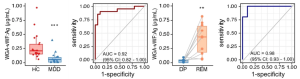
WGA結合性のフォンヴィレブランド因子(vWF)を含む血漿細胞外小胞(EV)(WGA-vWF)が、性別や年齢に関係なく、うつ病患者の診断マーカーとなり得ることが報告されました。
WGA-vWFの発現は、健康な対照参加者よりもうつ病状態の大うつ病性障害患者の血漿EVで有意に低下しています。 ROC分析により、大うつ病性障害患者とHC患者の間の診断のAUC値は0.92(95%CI 0.82~1.00)であることが示されました。更に、WGA-vWFの発現はうつ病から寛解の過程で顕著に増加しており、この結果を使用すると、うつ病状態と寛解状態の大うつ病性障害患者を区別することができました (AUC 0.98、95% CI 0.93 ~ 1.00)。