REQUIMTE-LAQV, Department of Chemistry, University of Aveiro, Portugalらのグループは、ビール酵母マイクロカプセル(BSY)を用いる経口ドラッグデリバリーシステムの可能性について述べています。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9857821/
BSYマイクロカプセルは、1M KOHまたは4M KOHによるアルカリ抽出法、または180℃或いは200℃での亜臨界水抽出(SWE)法を用いて抽出されました。得られたマイクロカプセルは、胃腸の消化状態を模倣したin vitro 消化 (IVD) で処理されました。消化されなかった物質は、マイクロカプセルの凝集と変形が見られるにもかかわらず、球形を維持し、(β1→3)-グルカンが豊富な構造となっていました。
SWE抽出マイクロカプセルのIVD処理から得られた可溶性多糖類はDectin-1と相互作用し、1M KOH抽出マイクロカプセルのIVD処理で放出されたものはDC-SIGNと相互作用し、4M KOH抽出および 180℃SWE抽出マイクロカプセル可溶化多糖類は、Dectin-2 と相互作用することが確認されました。
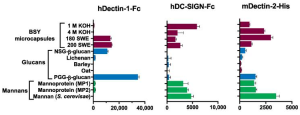
これらの結果は、生物医学的応用のための経口ドラッグデリバリーシステムとして、BSYマイクロカプセルが使用できるという可能性を示しています。
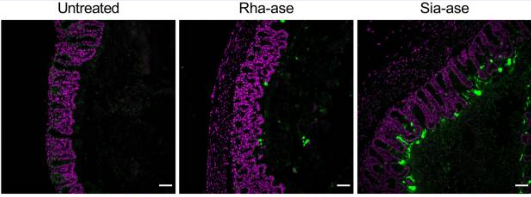 PNA staining in proximal colon
PNA staining in proximal colon