Swedish University of Agricultural Sciences, Uppsala, Swedenrらのグループは、細胞外多糖類を分泌する土壌バクテリアと共に、シリカ粒子を土壌に混ぜることによって、干ばつに強い小麦の根圏を作りました。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8229586/
今後10年の間に、農業は地球規模で大きな困難に直面することになります。それは地球規模での水資源の蒸発と降雨の減少による干ばつであり、降雨は地域によっても季節によっても気象変動により変化しています。世界の科学界は、限られたリソースの中で、どうやって小麦のような穀物植物の収穫を上げるかという問題に対して新規な方法を模索しており、幾つかの環境に優しい方法には大きなポテンシャルがあるのですが、大規模なフィールド応用に対しては注意深く最適化されねばなりません。そのような一つの方法が、植物の生長を促す根圏を用いて、植物の自然なディフェンス・システムを強化することなのです。植物の根圏を制御することによって、土壌細菌の相互作用を生かし、植物の生産性を回復させ、植物の環境変化に対する耐性を強化し、気象変動による影響を緩和することができるでしょう。
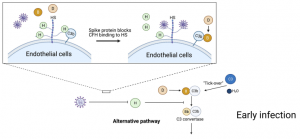
干ばつ耐性を向上させるために、まず初めに、土壌細菌A26に対して、4-phosphopantetheinyl transferaseを遺伝子的にノックアウトしたA26Sfpという株を作りました。A26Sfp株は、野生型のA26に比べて、グルクロン酸を主成分とする細胞外多糖類からなる菌膜の生産能力が向上しています。そもそも多糖類は親水性であり、保水能力を上げるにはとても適しています。
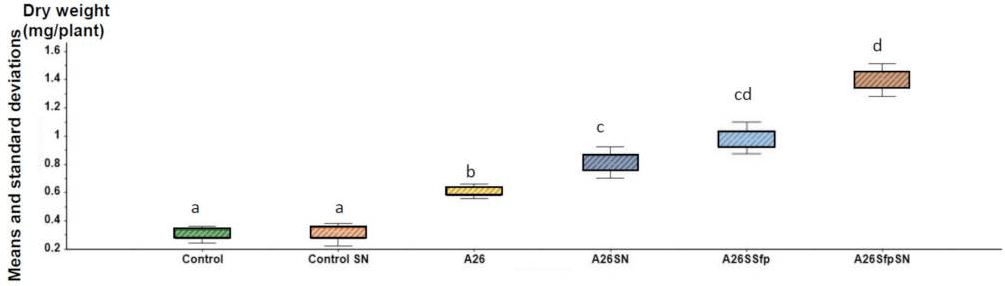
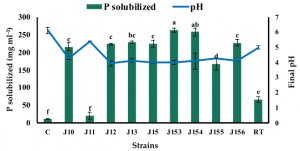
A26とA26Sfpを1/2 Tryptic soy broth (TSB)培地に50 µg/mL の濃度でシリカ粒子を加え、30℃で24時間培養しました。シリカ粒子の添加は、土壌細菌の数には影響を与えませんでしたが、細胞外多糖類の生産は、A26 と A26Sfp に対して、それぞれ46%、29%向上しました。A26Sfpの細胞外多糖類の生産は、その野生型A26に対して30–40%高くなっているのですが、シリカ粒子の点かで、それが更に20%増加しました。どうしてシリカ粒子の添加が、そのような効果を示すのかについては明確ではないのですが、形態的には細菌が長くなり、細菌集団の形成が見られ、これらが細胞外多糖類の産生増加に関係していると思われます。
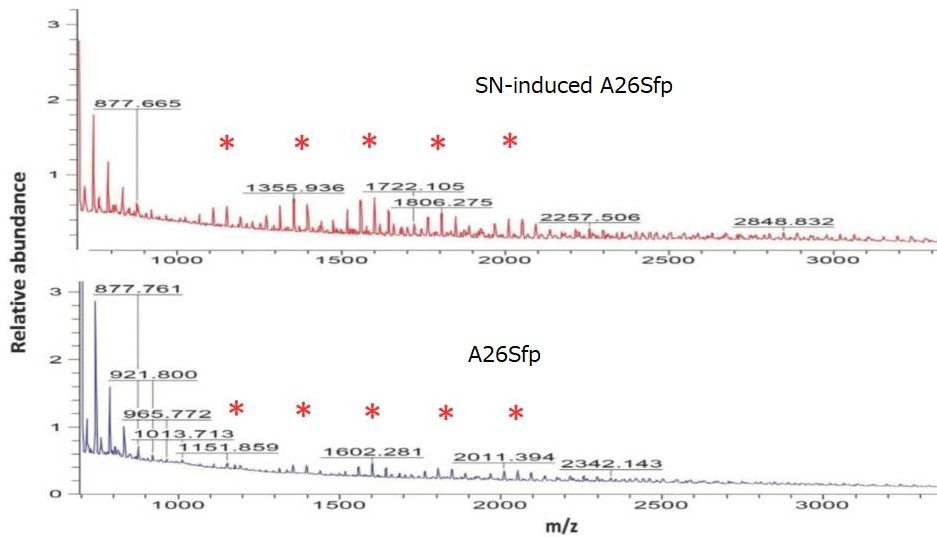
質量分析を用いて、細胞外多糖類の定量化を試みたところ、A26Sfpによって作られた細胞外多糖類が、野生型A26のそれに比べて長鎖構造になっていることが分かりました。長鎖の細胞外多糖類が土壌の保水力を上げる原因になっていることはほぼ間違いがないでしょう。