このブログ記事は、University of Bonn, GermanyらのCOVID-19における単球とマクロファージに関するレビュー論文から、そのエッセンスの紹介をしています。COVID-19においては、マクロファージはSARS-CoV-2を運ぶトロイの木馬と化し、単球はHLA-DRが減少し免疫抑制的に変貌して、末期癌や敗血症で見られる状態になっています。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8335157/
日々、肺は菌類、バクテリア、ウイルスら病原菌を多量に含んだ空気を数千リッターも吸い込んでいます。それらの感染や組織に発生する合併症を阻止する為には、免疫システムが厳格に制御されている必要があります。肺においては、恒常的な状態ではマクロファージが最も大量に存在する免疫細胞であります。マクロファージはその存在部位において、少なくとも二種の異なった集団が存在します。ひとつは、間質内マクロファージであり、もうひとつは肺胞マクロファージです。それらは、卵黄嚢に起源を持ち、誕生後初期から肺に存在します。肺胞マクロファージは増殖能力を持っており、骨髄からの供給を受けなくても、独立に自己再生によって生涯にわたって存在量を維持することができます。
ウイルス感染においては、肺胞マクロファージは初期の病原体認識、炎症の開始と制御、そして組織ダメージの修復に係わっています。肺胞マクロファージは、IL-1β、CCL3、CCL7、CCL2、MCP1らの細胞間伝達物質を多量に産生し、CCRを発現する骨髄由来の単球を急速に肺へと呼び寄せます。これは、必要な防御反応であり、ウイルスの攻撃によって、肺胞マクロファージやその派生種が大幅に減少することを補う必要があるからです。更に、肺胞マクロファージは、抗ウイルス反応を開始させる type I IFNを分泌する主役でもあります。
COVID-19 は、IL-1α、IL-1β、IL-6、IL-7、TNF、type I IFN、type II IFNらのサイトカイン、CCL2、CCL3、CXCL10らの炎症性ケモカインらの全体的な増加によって特徴付けられます。全体的なサイトカイン応答の増加というのはCOVID-19において議論の余地はないのですが、COVID-19の病理で使われるサイトカイン・ストームという言い方には、議論の余地があります、というのもTNF、IL-6、IL-8らのCOVID-19における濃度は、敗血症、COVID-19とは無関係な急性呼吸器不全症候群、重い外傷、心停止、そしてサイトカイン放出症候群(CRS)らと比べて高くないからなのです。重度のCOVID-19の患者で見られる全体的なサイトカインのプロファイルは、マクロファージ活性化症候群(MAS)と似ており、この事は、単核貪食細胞系(単球やマクロファージ)の異常がCOVID-19の過炎症に関係しているのではないかということを強く示唆します。
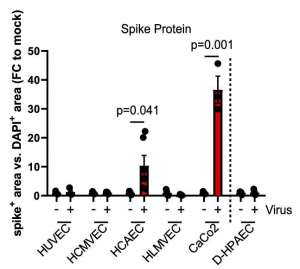
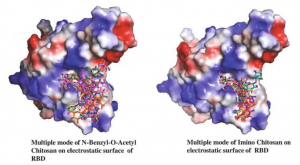
肺に存在する単核貪食細胞群へのSARS-CoV-2 感染というのは、肺胞上皮細胞の貪食後にリソソームから逃れたウイルスが感染、或いはまた直接的に感染していると考えられます。COVID-19における単核貪食細胞群からのサイトカインの産生は、パターン認識受容体(PRRs)によるSARS-CoV-2に感染した肺胞上皮細胞から放出される細胞損傷関連分子パターン(DAMPs)の認識、或いはまた、Toll様受容体を介した病原体関連分子パターン (PAMPs)の直接的な認識によって開始されます。更には、DC-SIGN、L-SIGNらのC-型レクチン、或いはTweety family member 2らがSARS-CoV-2 Spikeタンパク質と相互作用し、炎症性反応を誘起します。どうも、肺胞マクロファージがSARS-CoV-2を運ぶトロイの木馬のように作用しているようなのです。つまり、ウイルスに感染したマクロファージが近くの肺組織へウイルスを感染させ、それによってゆっくりとSARS-CoV-2の感染が広がり、肺全体に過炎症を引き起こすのです。
全ての研究事例を通じて最も特徴的なことは、COVID-19の重症患者では、単球のHLA-DRの発現が減少しているということなのです。このHLA-DRの減少というのは、COVID-19の重症度と強く相関しています。HLA-DRの減少というのは、単球系骨髄由来免疫抑制細胞(MDSC)においてみられる特徴であり、これは末期の癌や敗血症において見られるものであり、免疫抑制的な機能を持っています。COVID-19において、そのようなHLA-DRlo 単球が炎症性ケモカインによって肺へ呼び寄せられ、過剰に活性化された単核貪食細胞群が更に炎症性サイトカインやケモカインを分泌し、この連鎖的な反応が連続的に起こることで炎症を重くし、肺組織にダメージを与えていると考えられます。