Goethe University Frankfurt, Germanyらのグループは、ヒトの各種内皮細胞におけるSARS-CoV-2の感染のし易さについて報告しています。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8256413/
SARS-CoV-2 は主に肺胞上皮細胞に感染し、急性呼吸器不全症候群(ARDS)を引き起こします。しかしながら、内皮細胞機能不全や血管イベントがこの病気の主要な合併症であることも良く知られています。実際に、循環器系の炎症、障壁血管による組織浮腫、播種性血管内凝固の活性化および微小血栓が、COVID-19の中症から重症患者で報告されています。しかしながら、内皮細胞機能不全がSARS-CoV-2の内皮細胞への直接的な感染で起きているのか、サイトカインの放出による炎症カスケードの二次的な結果なのか?については、明確ではありません。
そこで、異なった血管床から得られた幾つかのヒトの内皮細胞をSARS-CoV-2と共培養し、それら内皮細胞への感染のし易さについて評価が行われました。評価された内皮細胞は次の通りです、
ヒト臍帯内皮細胞 (HUVEC)、
ヒト冠状動脈内皮細胞 (HCAEC)、
ヒト心臓微小血管内皮細胞 (HCMVEC)、
ヒト肺微小血管内皮細胞 (HLMVEC)。
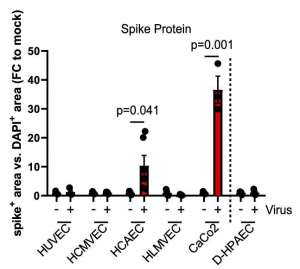
SARS-CoV-2 Spikeタンパク質は、ウイルス感染実験後、 ヒト冠状動脈内皮細胞から検出され、その他の内皮細胞からは検出されませんでした。この結果というのは、ウイルスの感染に必要とされるACE2を発現しているのは、ヒト冠状動脈内皮細胞のみであるという事実と相関しています。
ヒト大腸腫瘍細胞(CaCo2)がSARS-CoV-2感染のポジコンとして使用されています。
SARS-CoV-2 Spikeタンパク質は、ヒト冠状動脈内皮細胞から検出されましたが、このことは必ずしも内皮細胞に感染したということを意味するものではありません。それ故、RNA増幅の証拠となる二重らせんRNA、およびウイルス増殖の証拠となり得る細胞培養上清中のウイルスの存在が評価されました。しかしながら、SARS-CoV-2感染後5日間が過ぎても、ヒト冠状動脈内皮血管からは二重らせんRNAは検出されず、培養上清からもウイルスは検出されませんでした。このことは、ヒト冠状動脈内皮細胞にウイルスは取り込まれたが、その後全くウイルスは細胞内で増殖していないということを示すものです。
結果として、COVID-19で苦しむ患者に見られる多くの内皮細胞機能不全や微小血管内血栓らの合併症は、サイトカイン放出によって介在される炎症カスケードの結果として現れているものであり、内皮細胞への直接感染が原因ではないことが明らかになりました。