日本における新型コロナウイルスの第一波と第二波の違いについて調査した結果があります。
https://www.journalofinfection.com/article/S0163-4453(20)30693-9/fulltext
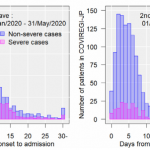
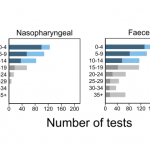
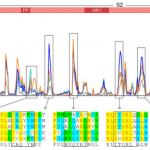
第一波は、2020年4月にピークを迎え、第二波は同年8月にピークを迎えています。第二波では、D614Gの変異により感染力が上がったと言われていますが、重症化率は下がっていることが如実に示されています。但し、第二波では、第一波に比べて若年層の感染者が多いということもあり、それが重症化率を下げている原因になっている可能性もあります。
既に、現在は第三波に入っていると言われており、更にどのような変化が感染力や重症化に起こっているのかが注目されます。