Harvard Medical School, USAらのグループは、COVID-19の患者では、血中の単球の10%、肺のマクロファージの8%がSARS-CoV-2に感染しており、Fc受容体を介して抗体・ウイルス結合体が取り込まれることによって誘起される炎症性細胞死(パイロトーシス)がCOVID-19にとって諸刃の剣になっていると述べています。
https://www.researchsquare.com/article/rs-153628/v1
SARS-CoV-2がどのようにして炎症を引き起こすのかについて、未だにその全容が完全に理解されておりません。
単球とマクロファージは、それぞれ、血中および組織における、免疫の最前線にいる免疫細胞であります。これら免疫細胞は、ウイルスの侵入を感知すると、インフラマソームを形成し、caspase-1やガスダーミンD (GSDMD) を活性化し、炎症性細胞死を誘起するとともに、炎症性サイトカインを放出します。
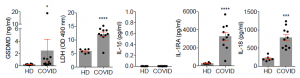
単球は、一般的にACE2は発現していないとされ、実際、健常者(HD)の単球も、SARS-CoV-2によって活性化された単球においても、ACE2の発現はフローサイトメータでもqRT-PCRでも確認されませんでした。単球には2種のFcg受容体が存在します、一つはCD32(FcgRII、ほとんどの血中単球に存在)であり、もう一つはCD16(FcgRIII、COVID-19の患者で発現)であります。これらの受容体は、抗体・ウイルス結合体を認識し、抗体依存性貪食作用(ADP)によってウイルスを取り込みます。パイロトーシスや他の細胞壊死の病理的な特徴としては、LDHのような巨大分子の放出があります。実際、LDHの上昇は、重度のCOVID-19と優れた相関を示し、血中のGSDMD、IL-1RA、IL-18も重度のCOVID-19で顕著に増加、GSDMD eOTLsは、COVID-19の急性呼吸器不全と最も顕著に相関していました。
ウイルスを取り込んだ後、SARS-CoV-2は単球内で増殖しており、実際、dsRNAの検出などによりそのことは確認されました。しかしながら、感染は中断され、感染された細胞は、NLRP3、AIM2 inflammasome、caspase-1 、GSDMDらの活性化を介して炎症性細胞死を遂げます。更に、COVID-19で病死した患者の肺の検死から得られた肺胞マクロファージは、同じようなインフラマソーム活性化を示していました。これらのことを総合すると、抗体を介したSARS-CoV-2の単球やマクロファージの感染が、炎症性細胞死を引き起こし、それによってウイルスの増殖は止まるのですが、同時に炎症性サイトカインを放出し、COVID-19の重症化につながっていると考えられます。