Department of Mathematics, Michigan State University, MI, USAらのグループは、SARS-CoV-2 オミクロン変異株の感染力、ワクチンブレークスルー、抗体医薬に対する影響力の評価結果を報告しています。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8647651/
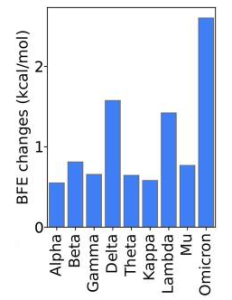
感染力:
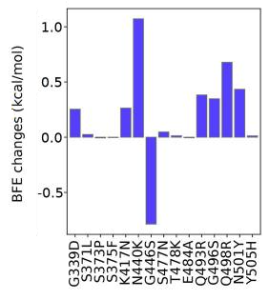
SARS-CoV-2の感染力は、主にACE2とRBD複合体の結合親和性によって決定されますが、furin切断部位も重要な役割を果たします。オミクロンは、furin切断部位に3つの変異があり、RBDに15の変異があることから、感染力には有意な変化があることが示唆されます。オミクロンの感染力の変化は、15個のRBD変異によって誘発されるACE2およびSpikeタンパク質複合体の結合自由エネルギー(BFE)の変化を調べることによって分析されました。その結果、オミクロンはデルタの約2.8倍の感染力を持つと考えられます(BFEの変化:1.57kcal / mol)。
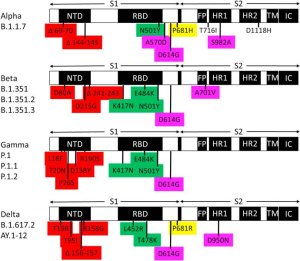
ワクチンブレークスルー:
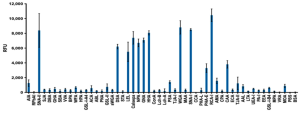
ワクチンに対するオミクロンの影響を、132個の既知の抗体とSpikeタンパク質複合体のライブラリを用いて分子ベースのデータ駆動型分析によって評価しました。これらの複合体の15個のRBD変異によって誘発される結合自由エネルギーの変化を評価して、ワクチンに対するオミクロンのRBD変異の潜在的な影響が見えてきます。この研究では、抗体ライブラリーの実験データが限られているため、RBDから離れた既知の抗体-Spikeタンパク質複合体(N末端ドメイン(NTD)の複合体など)はこの評価には含まれていません。その結果、オミクロンのワクチンエスケープ能力は、デルタの約2倍になっていると考えられます。
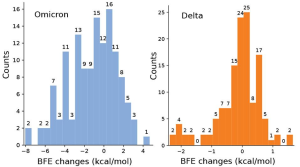
抗体医薬への影響:
オミクロンは、Regeneronの抗体カクテル医薬については、それほど大きな影響は出ないであろうと考えられます。