Department of Medicine, University of Pennsylvania, Philadelphia, PA, USA らのグループは、脂質ナノ粒子(LNP)が、アジュバントとしてワクチンの有効性を高めるということをインフルエンザのヘマグルチニンと、SARS-CoV-2のRNAを用いて示しています。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8566475/
アジュバントは、ワクチン接種に対する適応免疫応答の質と大きさを改善するために重要です。 LNPカプセル化ヌクレオシド修飾mRNAワクチンは、SARS-CoV-2の重症急性呼吸器症候群に対して優れた効果を示していますが、このワクチンプラットフォームの作用機序は十分に解明されていません。
このLNPがアジュバント活性を持つことを実証するために、空のLNP(eLNP)およびAddaVaxアジュバントSARS-CoV-2 Spikeタンパク質サブユニットワクチンを用いました。マウスをeLNPまたはAddaVaxでアジュバント添加された組換えSARS-CoV-2 Spikeタンパク質受容体結合ドメイン(rRBD)の単回投与で免疫し、陽性対照として、もうひとつのグループをヌクレオシド修飾RBD mRNA-LNPで免疫しました。結果、LNPアジュバントワクチンは、AddaVaxアジュバントによって誘発された応答よりも有意に高いRBD特異的IgG力価を誘発することが示されました。
イオン化可能な脂質がある場合とない場合のLNPのアジュバント特性を比較するために、2つの異なる組成を持つeLNPと混合した組み換えヘマグルチニン(rHA)でマウスを免疫しました。イオン化可能な脂質を含むeLNPは、高い血球凝集素阻害力価を示しましが、驚くべきことに、イオン化可能な脂質を含まないeLNPはアジュバント活性を持っていませんでした。
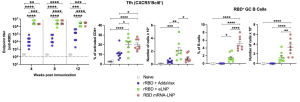
IL-6は、T濾胞ヘルパー細胞(Tfh)分化の初期調節因子であることが知られています。Tfh細胞は、胚中心(GC)におけるB細胞の親和性成熟の調節に特化したCD4+ T細胞のサブセットであり、Tfh細胞の誘導は、持続性のある免疫応答にとって非常に重要です。イオン化可能な脂質を含むeLNPとmRNA-LNPは、大量の炎症性サイトカイン(IL-6など)とケモカインを誘発するのに対し、イオン化可能な脂質を欠くLNPとAddaVaxでは、低いレベルの炎症性サイトカインとケモカインの誘導に留まりました。