東京都健康長寿研究センターらのグループは、心筋梗塞後の治療に、皮質骨由来幹細胞(CBSC)を用いた方が、間葉系幹細胞(MSC)を用いた再生医療よりも効果的であると述べています。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8584423/
最近、マウスを用いた実験で、皮質骨由来幹細胞(mCBSC)が心筋構造リモデリングに有効であることが示されています。mCBSCを用いることで、血管新生が増加し、新たな心筋細胞が作られることが示されています。mCBSCs の処理によって免疫調整機能と血管新生促進作用が特徴的に誘起されるようであり、このことが、心筋梗塞後の治療において、CBSCを用いた方がMSCよりも何故効果的なのかという理由の背景にありそうです。
mCBSCの自己再生能力はmMSCよりも高いのですが、mCBSCの分化能力はmMSCとは異なり、軟骨形成に高いようです。そしてまた、mCBSCsは、TGF-β1をmMSCよりもかなり多く分泌し、TGF-β1は、mCBSCマイグレーションを促すとともに、線維芽細胞の活性化にも寄与します。つまり、TGF-β1 を分泌するCBSCが心筋梗塞部へマイグレートし、心臓線維芽細胞を筋繊維芽細胞へ変化させているのかも知れません。
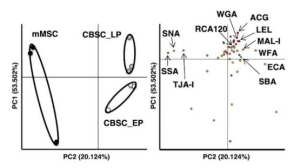
それら細胞表面の糖鎖については、WFA(lacdiNAc)、ECA(lactosamine-binding lectin)、MAL-I(α2-3 sialic acid binding lectin)の3つのレクチンが mCBSCs において、mNSCよりも高発現しており、SNA、SSA、TJA-I(α2-6 sialic acid binding lectins)らのレクチンが mCBSCs において、mMSCよりも顕著に低発現になっていました。つまり、α2-6sialic acid の低発現ということが、mCBSCの分化をより軟骨形成系統にしている原因なのかも知れません。
過去の研究では、糖鎖がPleukemia inhibitory factor (LIF)、Wnt、FGF、bone morphogenetic protein BMP、Notchらが介在するシグナル経路の制御に関係していることが示されており、LIF受容体βやgp130上のWFA結合性糖鎖がLIF/STAT3 シグナリングに関わり、そしてそれがマウスのES細胞の自己再生に必要であるということが示されています。
本研究においては、WFAに結合する糖鎖がCBSCに対してMSCよりもより特異的であり、これらの事柄は、WFA特異的な糖鎖が、LIF/STST3経路を活性化することによって、CBSCの自己再生能力を高めているのではないか?ということを示唆しているようです。