The Scripps Research Instituteは、SARS-CoV-2 Spikeタンパク質のナノ粒子を用いることで、ウイルスの変異にも強い広域中和抗体を作ることができるとしています。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8010731/
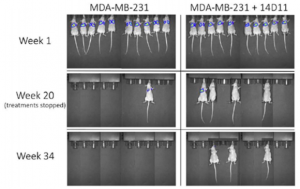
現在のワクチンの主流は、recombinant SARS-CoV-2 spikeを抗原として提示する形のプラットフォームであり、mRNAを包含したリポソーム (例えば, BNT162b2 や mRNA-1273)、アデノ随伴ウイルス・ベクターを用いたもの (例えば, ChAdOx1 nCoV-19 [AZD1222], CTII-nCoV, Sputnik V, や Ad26.COV2.S)らが存在します。これらのワクチンは、B.1.1.7変異についてはまだしも、B.1.351やP.1変異に対しては、有効性が顕著に低下することが指摘されています。従って、ウイルス変異に強い広域中和抗体を作ることが出来るワクチンが切望されており、その為には、成熟した抗体を長期間にわたって生み出せる胚中心の形成が必要不可欠です。
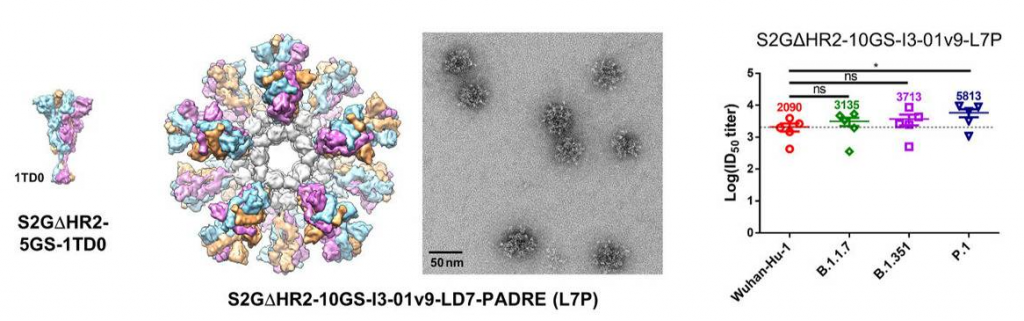
SARS-CoV-2 spikeタンパク質は、S1-S2ヘテロダイマーの三量体を形成しています。S1 subunitには、感染をイニシエートするRBDが含まれており、S2 subunitには、fusion peptide (FP) と heptad repeat regions 1 と 2 (HR1 と HR2)が含まれています。著者らは、Spikeタンパク質の安定性を高めるためにHR2-deleted, glycine-cappedのspikeタンパク質をデザインし (S2GΔHR2)、I3–01v9 60-mersをリンカーとしてナノ粒子化したS2GΔHR2-10GS-I3-01v9-LD7-PADRE (I3-01v9-L7P)をワクチンとして使用しました。I3-01v9-L7Pには、20個のS2GΔHR2が含まれています。
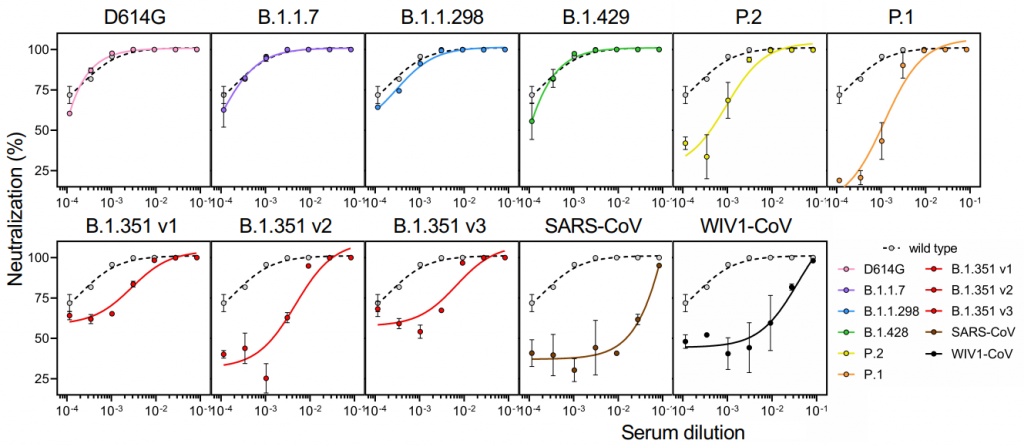
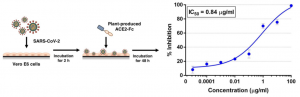
S2GΔHR2-10GS-I3-01v9-L7Pをワクチンとして使用することで、B.1.1.7, B.1.351, P.1 変異に対してほぼコンパチブルな力価を有する広域中和抗体が生成されていることがわかりました。このナノ粒子は、単体Spikeに比べて、6倍長い保持時間、4倍大きい濾胞樹状細胞群、5倍高い胚中心の活動を示しました。この理由については、定かではありませんが、ワクチンのサイズ効果だと推測されます。