Perelman School of Medicine, University of Pennsylvaniaらのグループは、高感度で高速検出な電気化学反応を利用した新型コロナウイルス検出のPOCTデバイス(RAPIDと命名)をプレゼンしています。
https://pubmed.ncbi.nlm.nih.gov/33997767/
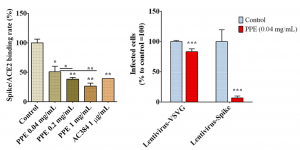
SARS-CoV-2 Spikeタンパク質を検出するためにACE2がプローブとして使用されています。ACE2を電極上に固定化するために、二官能性化合物であるグルタルアルデヒドをリンカーとして使用し、BSAを用いてノンスペをブロッキングします。感度を上げるために、ナフィオンも使用されました。
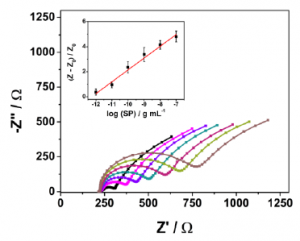
ACE2 と SARS-CoV-2 Spikeタンパク質の結合が、ここで使用されているRedoxプローブ(ヘキサシアノ鉄酸塩)と電極間の電荷の流れに影響を及ぼすことを利用して、その電荷移動抵抗の変化を測定することで検出します。
結果として、10 fg/mL から 100 ng/mL の範囲で線形な反応を得ることが出来 (R2 = 0.993)、検出限界は2.18 fg/mL (S/N=3)となりました。測定時間も4分と非常に高速です(サンプルのインキュベーションに2分、測定と解析に2分)。
139 鼻腔swabサンプルを用いたブラインドテストでは(109は、RT-PCRでCOVID-19陽性、内30は、RT-PCRで陰性)、感度、特異度、正確性は鼻腔Swabサンプルで、それぞれ83.5%、100%、87.1%となり、唾液サンプルで、それぞれ100%、86.5%、90.0%となりました。