Institute of Physiology, University of Zurich, Zurich, Switzerlandのグループは、レクチンの細胞毒性について報告しています。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8866831/
レクチンによる細胞表面糖鎖の標的化は癌治療の有望なアプローチですが、レクチンベースのアプローチ(レクチン単独または他の治療薬との組み合わせ)はまだ開発の初期段階にあります。糖鎖ターゲティングに基づく効率的な治療法の開発には、標的腫瘍細胞上のレクチンによって誘発される細胞死のメカニズムを深く理解する必要があります。特定のレクチンが異なるタイプの腫瘍細胞で異なるモードの細胞死を誘発することが知られています。たとえば、小麦胚芽レクチン(WGA)は、メラノーマと白血病細胞にアポトーシスを誘導し、パラトーシスのような細胞死によって頸部癌細胞を殺すことなどが知られています。
本研究においては、マウス腺癌細胞(MC-38)と若い成体マウス結腸細胞(YAMC)を使用して、レクチン(MAL I、MAL II、SNA、AAL、WGA、およびECL)処理によって誘起される様々な細胞死経路(アポトーシス、ネクロトーシス、パイロトーシス、パラトーシス、およびオートファジー依存性細胞死)が評価されました。レクチンの細胞毒性によって誘導される細胞死を媒介するシグナル伝達経路を判別するために、細胞死応答に関与する様々な遺伝子をノックアウトしたMC-38細胞のパネルを使用しています。
ノックアウトされた遺伝子は次の通りです:
アポトーシス促進タンパク質BCL2アンタゴニスト/キラー1(BAK1)およびBCL2関連X(BAX)は、内因性アポトーシスを媒介します、内因性アポトーシスのシグナル経路は、DNA損傷などのさまざまな内部細胞ストレス因子に応答して活性化されます。
Fas結合デスドメインタンパク質(FADD)は、外因性アポトーシスを媒介します、外因性アポトーシス経路は、細胞死受容体の活性化に応答して誘導され、その後、 FADDとプロカスパーゼ-8を含む細胞死誘導シグナル伝達複合体を形成し、カスパーゼ-3を切断します。
腫瘍ネクローシス因子受容体1型結合デスドメインタンパク質(TRADD)、受容体相互作用セリン/スレオニンプロテインキナーゼ3(RIPK3)、混合系統キナーゼドメイン様タンパク質(MLKL)およびカスパーゼ-8(CASP8)は、カスパーゼ非依存性ネクロトーシスを媒介します。
カスパーゼ-1(CASP1)とガスデルミンD(GSDMD)は、パイロトーシスを媒介します、CASP1は、様々な微生物感染や非感染性の刺激に応答してインフラマソームによって活性化されます。この経路はGSDMD切断につながり、これが原形質膜に埋め込まれて細孔ができることで、イオン勾配を乱して水の流入を促進し、細胞の腫れと浸透圧溶解を引き起こします。
結果:
BAX/BAK1複合体の不活性化は、WGA、MAL I、およびAAL処理によって誘発される細胞毒性反応を減少させました。細胞毒性の50%以上の減少は、アポトーシスの古典的なトリガーであるシスプラチンで処理された細胞でみられる効果と同様でした。対照的に、FADDの不活性化は、WGA、MAL I、およびAALによって媒介される細胞死に影響を与えませんでした。
腫瘍壊死因子受容体1(TNFR1)の下流のアポトーシスとネクロトーシスの活性化に必要な別のアダプター分子であるTRADDの不活性化は、MAL Iで処理した細胞の細胞死を減少させましたが、WGAとAALの場合には減少しませんでした。 MLKLの低下が、WGA、MAL I、およびAALの細胞毒性効果を減少させることから、これらレクチンによって誘発される細胞死にネクロトーシス経路が寄与していることが示唆されます。
CASP1またはGSDMDのいずれかの不活化は、MAL Iを介した細胞毒性のわずかな減少のみを示し、MAL I処理に応答したパイロトーシスの部分的な関与を裏付けています。 CASP1の不活化は、MALおよびAALによって誘発される細胞毒性の低下をもたらしました。
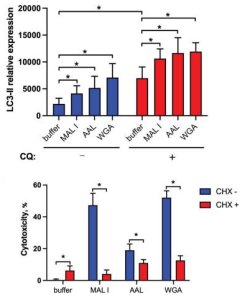
アポトーシスの誘導に加えて、多くのレクチンはオートファジーを昂進させ、オートファジー依存性の細胞死を引き起こすことがあります。 LC3-IIはオートファゴソーム膜に関連していまが、レクチンで6時間処理した細胞からの溶解物において、MAL I、AAL、およびWGA処理でLC3-IIの発現が昂進していました。 LC3-IIの増加は、MAL I、AAL、およびWGAによって誘導される細胞死が、古典的なアポトーシスミトコンドリア経路ではなく、オートファジー/リソソーム応答の活性化によって開始された可能性があることを示しています。実際、飢餓によって誘発されるオートファジーを阻害することが知られているシクロヘキシミド(CHX)を添加することにより、3つのレクチンの細胞毒性反応が大幅に低下しました。